NCERT Solutions of Science in Hindi for Class 10th: Ch 4 कार्बन एवं उसके यौगिक विज्ञान
प्रश्नपृष्ठ संख्या 68
1. CO2 सूत्र वाले कार्बन डाइआँक्साइड की इलेक्ट्रान बिन्दु संरचना क्या होगी?
उत्तर
C की परमाणु संख्या = 6 इलेक्ट्रॉनिक विन्यास = 2, 4
O की परमाणु संख्या = 8 इलेवट्रॉनिक विन्यास = 2, 6
इलेवट्रॉन बिन्दु संरचना
कार्बन एवं उसके यौगिक

2. सल्फर के आठ परमाणुओं से बने सल्फर के अणु की इलेक्ट्रान बिन्दु संरचना क्या होगी? (संकेत : सल्फर के आठ परमाणु एक अँगूठी के रूप में आपस में जुड़े होते हैँ।)
उत्तर
सल्फर (S) की परमाणु संख्या द्वार =16

पृष्ठ 76
1. पेन्टेन के लिए आप कितने संरचनात्मक समावयवियों का चित्रण कर सकते हैं?
उत्तर
C5H12 (पेन्टेन) के तीन संरचनात्मक समावयदी सम्भव है|

नोट: समयावता (Isomerism) वह परिघटना जिसमें एक अणुसूत्र वाले एक से अधिक यौगिक पाए जाते है जिनके गुणधर्म सामान्यतया भिन्न-भिन्न होते हैं|
2. कार्बन के दो गुषाघर्म कौन-कौन से हैं, जिनके कारण हमारे चारों ओर कार्बन यौगिकों की विशाल संख्या दिखाई देती है?
उत्तर
कार्बन एक विशाल संख्या में योगिक बनाता है। इसक दो मुख्य कारण निम्न हैं|
श्रृंखलन: कार्बन में कार्बन के ही अन्य परमाणुओं के साथ आबंध बनाने की अद्वितीय क्षमता होती है जिससे बड़ी संख्या में अणु बनते हैं| इस गुण को श्रृंखलन कहते हैं|
चतु:संयोजकता: चूँकि कार्बन की संयोजकता चार होती है, अतः इसमें कार्बन के चार अन्य परमाणुओं अथवा कुछ अन्य एक संयोजक तत्वों के परमाणुओं के साथ आबंधन की क्षमता होती है|
3. साइक्लोपेन्टेन का सूत्र तथा इलेक्ट्रॉन बिंदु संरचना क्या होंगे?
उत्तर
साइक्लोपेन्टेन का सूत्र C5H10 है| इसकी इलेक्ट्रॉन बिंदु संरचना नीचे दी गई है:

4. निम्न यौगिकों की संरचनाएँ चित्रित कीजिए :
(i) एथेनॉइक अम्ल
(ii) ब्रोमोपेन्टेन*
(iii) ब्यूटेनोन
(iv) हेक्सेनैल
*क्या ब्रोमोपेन्टेन के संरचनात्मक समावयव संभव हैं?
उत्तर
(i) एथेनोइक अम्ल (CH3COOH)

(ii) ब्रोमोपेन्टेन (CH3CH2CH2CH2CH2Br)

(iii) ब्यूटेनॉन (CH3CH2COCH3)

(iv) हेक्सेनैल (CH3CH2CH2CH2CH2CHO)
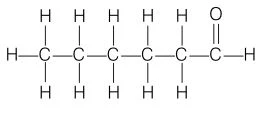
(ii) ब्रोमोपेन्टेन के अनेक संरचनात्मक समावयव संभव हैं| उनमें से तीन संरचनात्मक समावयव दिए गए हैं :

5. निम्न यौगिकों का नामकरण कैसे करेंगे?
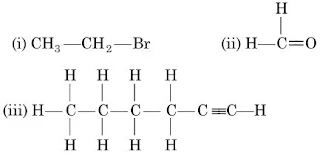
उत्तर
(i) ब्रोमोपेन्टेन
(ii) मेथेनल
(iii) हेक्सेन
पृष्ठ संख्या 79
1. एथनॉल से एथेनॉइक अम्ल में परिवर्तन को ऑक्सीकरण अभिक्रिया क्यों कहते हैं?
उत्तर
CH3CH2OH + (क्षारीय KMnO4) → CH3COOH
चूँकि इस अभिक्रिया में एथनॉल में एक ऑक्सीजन का संकलन होता है, इसलिए यह ऑक्सीकरण अभिक्रिया कहलाता है|
2. ऑक्सीजन तथा एथाइन के मिश्रण का दहन वेल्डिंग के लिए किया जाता है| क्या आप बता सकते हैं कि एथाइन तथा वायु के मिश्रण का उपयोग क्यों नहीं किया जाता?
उत्तर
2HC ≡ CH + 5O2 → 4CO2 + 2H2O + ऊष्मा
जब एथाइन का दहन वायु की उपस्थिति में किया जाता है तो यह कज्जली ज्वाला उत्पन्न करता है| यह वायु की आपूर्ति को सीमित कर देने से अपूर्ण दहन होने के कारण होता है| जबकि, यदि एथाइन का दहन ऑक्सीजन में किया जाता है तो यह संपूर्ण दहन के कारण तापमान 3000 डिग्री सेल्सियस के साथ एक स्वच्छ लौ देता है| वेल्डिंग के लिए आवश्यक उच्च ऊष्मा उत्पन्न करने के उद्देश्य से एथाइन का पूर्ण दहन ऑक्सीजन की उपस्थिति में किया जाता है|
पृष्ठ संख्या 82
1. प्रयोग द्वारा आप एल्केहॉल तथा कार्बोक्सिलिक अम्ल में कैसे अंतर कर सकते हैं?
उत्तर
हम कार्बोनेट और हाइड्रोजनकार्बोनेट के साथ उनकी अभिक्रिया के आधार पर एल्केहॉल तथा कार्बोक्सिलिक अम्ल के बीच अंतर कर सकते हैं| अम्ल कार्बोनेट और हाइड्रोजनकार्बोनेट से CO2 गैस उत्सर्जित करने के लिए अभिक्रिया करता है, जो चूने का पानी को दूधिया करता है|
कार्बोनेट/ हाइड्रोजनकार्बोनेट + कार्बोक्सिलिक अम्ल → लवण + जल + कार्बन डाइऑक्साइड
वहीँ दूसरी ओर, एल्केहॉल कार्बोनेट और हाइड्रोजनकार्बोनेट के साथ अभिक्रिया नहीं करता है|
2. ऑक्सीकारक क्या हैं?
उत्तर
कुछ पदार्थों में अन्य पदार्थों को ऑक्सीकरण के लिए ऑक्सीजन देने की क्षमता होती है या हाइड्रोजन को अलग करने में सहायक होते हैं, वे ऑक्सीकारक कहलाते हैं|
पृष्ठ संख्या 85
1. क्या आप डिटरजेंट का उपयोग कर बता सकते हैं कि कोई जल कठोर है अथवा नहीं?
उत्तर
डिटरजेंट कठोर और मृदु दोनों प्रकार के जल के साथ झाग उत्पन्न करता है, जबकि साबुन मृदु जल के साथ ही झाग उत्पन्न करता है| इसलिए डिटरजेंट का उपयोग कर यह बता पाना कि कोई जल कठोर है अथवा नहीं, असंभव है|
2. लोग विभिन्न प्रकार से कपड़े धोते हैं| सामान्यतः साबुन लगाने के बाद लोग कपड़े को पत्थर पर पटकते हैं, डंडे से पीटते हैं, ब्रुश से रगड़ते हैं या वाशिंग मशीन में कपड़े रगड़े जाते हैं| कपड़ा साफ़ करने के लिए उसे रगड़ने की क्यों आवश्यकता होती है?
उत्तर
एक साबुन के अणु के दो भाग होते हैं, जिसे जलरागी तथा जलविरागी कहते हैं| इसके सहायता से तैलीय मैल मिसेल के केंद्र में एकत्र हो जाते हैं| मिसेल विलयन में कोलाइड के रूप में बने रहते हैं| इस मिसेल को हटाने के लिए कपड़ों को रगड़ना आवश्यक होता है|
पृष्ठ संख्या 86
1. एथेन का आण्विक सूत्र –C2H6 है| इसमें :
(a) 6 सहसंयोजक आबंध है|
(b) 7 सहसंयोजक आबंध है|
(c) 8 सहसंयोजक आबंध है|
(d) 9 सहसंयोजक आबंध है|
उत्तर
(b) 7 सहसंयोजक आबंध है|
2. ब्यूटेनॉन चर्तु-कार्बन यौगिक है जिसका प्रकार्यात्मक समूह
(a) कार्बोक्सिलिक अम्ल
(b) ऐल्डिहाइड
(c) कीटोन
(d) एल्कोहॉल
उत्तर
(c) कीटोन
3. खाना बनाते समय यदि बर्तन की तली बाहर से काली हो रही है तो इसका मतलब है कि
(a) भोजन पूरी तरह नहीं पका है|
(b) ईंधन पूरी तरह से नहीं जल रहा है|
(c) ईंधन आर्द्र है|
(d) ईंधन पूरी तरह से जल रह है|
उत्तर
(b) ईंधन पूरी तरह से नहीं जल रहा है|
4. CH3Cl में आबंध निर्माण का उपयोग कर सहसंयोजक आबंध की प्रकृति समझाइए|
उत्तर

कार्बन में संयोजकता इलेक्ट्रॉनों की संख्या चार होती है| इसके 1 इलेक्ट्रॉन हाइड्रोजन के तीन अणु के साथ तथा 1 इलेक्ट्रॉन क्लोरीन के साथ साझेदारी करते हैं| कार्बन तथा क्लोरीन के अणुओं के बीच सहसंयोजी आबंध होता है लेकिन क्लोरीन की उच्च विद्युत ऋणात्मकता के कारण कार्बन तथा क्लोरीन के आबंध की प्रकृति ध्रुवीय होती है|
5. इलेक्ट्रॉन बिंदु संरचना बनाइए :
(a) एथेनॉइक अम्ल
(b) H2S
(c) प्रोपेनोन
(d) F2
उत्तर
(a) एथेनॉइक अम्ल

(b) H2S

(c) प्रोपेनोन

(d) F2

कार्बन में संयोजकता इलेक्ट्रॉनों की संख्या चार होती है| इसके 1 इलेक्ट्रॉन हाइड्रोजन के तीन अणु के साथ तथा 1 इलेक्ट्रॉन क्लोरीन के साथ साझेदारी करते हैं| कार्बन तथा क्लोरीन के अणुओं के बीच सहसंयोजी आबंध होता है लेकिन क्लोरीन की उच्च विद्युत ऋणात्मकता के कारण कार्बन तथा क्लोरीन के आबंध की प्रकृति ध्रुवीय होती है|
6. समजातीय श्रेणी क्या है? उदाहरण के साथ समझाइए|
उत्तर
यौगिकों की ऐसी श्रृंखला जिसमें कार्बन श्रृंखला में स्थित हाइड्रोजन को एक ही प्रकार का प्रकार्यात्मक समूह स्थापित करता है, उसे समजातीय श्रेणी कहते हैं| उदाहरण के लिए, मिथेन, एथेन, प्रोपेन, ब्यूटेन एल्कीन की समजातीय श्रेणी हैं|
मिथेन: CH4
एथेन: CH3CH3
प्रोपेन: CH3CH2CH3
ब्यूटेन: CH3¬CH2CH2CH3
यह देखा जा सकता है कि प्रत्येक उत्तरोत्तर यौगिकों के बीच -CH2 इकाई का अंतर है|
7. भौतिक एवं रासायनिक गुणधर्मों के आधार पर एथनॉल तथा एथेनॉइक अम्ल में कैसे अंतर करेंगे?
उत्तर
• एथनॉल एक विशेष गंध के साथ कमरे के तापमान पर द्रव अवस्था में होता है| एथेनॉइक अम्ल का गलनांक बिंदु 17°C होता है| चूँकि यह कमरे के तापमान से कम है, इसलिए शीत के दिनों में यह जम जाता है| साथ ही एथेनॉइक अम्ल की गंध सिरके की तरह होती है|
• एथनॉल कार्बोनेट धातु के साथ अभिक्रिया नहीं करता है, जबकि एथानॉइक अम्ल धातु कार्बोनेट धातु से अभिक्रिया कर लवण, जल तथा कार्बन डाइऑक्साइड बनाता है|
2CH3COOH + Na2CO3 → 2CH3COONa + CO2 + H2O
• एथनॉल सोडियम हाइड्रोक्साइड के साथ अभिक्रिया नहीं करता है जबकि एथानॉइक अम्ल सोडियम हाइड्रोक्साइड के साथ अभिक्रिया करके सोडियम एथेनॉइट तथा जल बनाता है|
CH3COOH + NaOH → CH3COONa + H2O
8. जब साबुन को जल में डाला जाता है तो मिसेल का निर्माण क्यों होता है? क्या एथनॉल जैसे दूसरे विलायकों में भी मिसेल का निर्माण होगा?
उत्तर
साबुन के अणु के दो सिरे होते हैं| एक सिरा जलरागी तथा दूसरा सिरा जलविरागी होता है| जब साबुन को जल में घोला जाता है तथा कपड़े को साबुन के विलयन में डाला जाता है तो तैलीय धूल के कण हाइड्रोकार्बन भाग से तथा जल के अणु आयनिक भाग से जुड़ जाते हैं| अब ये सभी साबुन के अणुओं के आयनिक (ऋणात्मक) भाग बाहर की ओर तथा हाइड्रोकार्बन भाग भीतर की ओर व्यवस्थित होकर मिसेल बनाते हैं| ये कोलाइड के रूप में रहते हैं तथा आयन-आयन विकर्षण के कारण अवक्षेपित नहीं होते|
एथनॉल जैसे दूसरे विलायकों में मिसेल का निर्माण नहीं होता क्योंकि साबुन की तरह इनकी प्रकृति ध्रुवीय नहीं होती|
9. कार्बन एवं उसके यौगिकों का उपयोग अधिकतर अनुप्रयोगों में ईंधन के रूप में क्यों किया जाता है?
उत्तर
कार्बन एवं उसके यौगिकों में कार्बन तथा हाइड्रोजन का प्रतिशत उच्च होने के कारण दहन करने पर प्रचुर मात्रा में ऊष्मा उत्पन्न करते हैं| ईंधन के रूप में उपयोग किए जाने वाले कार्बन तथा उसके यौगिकों का उच्च कैलोरी मान के साथ अनुकूलतम प्रज्वलन तापमान होता है तथा उन्हें नियंत्रित करना आसान होता है| इसलिए कार्बन एवं उसके यौगिकों का उपयोग अधिकतर अनुप्रयोगों में ईंधन के रूप में किया जाता है|
10. कठोर जल को साबुन से उपचारित करने पर झाग के निर्माण को समझाइये|
उत्तर
कठोर जल में कैल्शियम तथा मैग्नीशियम के लवण उपस्थित होते हैं| साबुन के अणु कैल्शियम तथा मैग्नीशियम के लवण के साथ अभिक्रिया कर अवक्षेपण का निर्माण करते हैं| यह अवक्षेपण जल के ऊपर सफ़ेद परत के रूप में तैरता रहता है| यह परत अघुलनशील पदार्थ स्कम कहलाता है| स्कम के निर्माण के कारण साबुन कठोर पानी में अपनी सफाई की प्रवृत्ति खो देता है|
11. यदि आप लिटमस पत्र (लाल एवं नीला) से साबुन की जाँच करें तो आपका प्रेक्षण क्या होगा?
उत्तर
चूँकि साबुन की प्रकृति क्षारीय होती है इसलिए लाल लिटमस पत्र नीले रंग में परिवर्तित हो जाएगा| जबकि नीला लिटमस पत्र नीला ही रहेगा|
12. हाइड्रोजनीकरण क्या है? इसका औद्योगिक अनुप्रयोग क्या है?
उत्तर
हाइड्रोजनीकरण उत्प्रेरक की उपस्थिति में हाइड्रोजन और अन्य यौगिकों के बीच रासायनिक अभिक्रिया है| हाइड्रोजनीकरण का उपयोग मुख्य रूप से असंतृप्त हाइड्रोकार्बन को कम करने के लिए किया जाता है| हाइड्रोजनीकरण एक अतिरिक्त अभिक्रिया है| उदाहरण के लिए, जब एथेन को निकेल उत्प्रेरक के साथ गर्म किया जाता है तो यह एथेन तक कम हो जाता है|
औद्योगिक उपयोग :
• हाइड्रोजनीकरण का उपयोग पेट्रो-रसायन उद्योगों में ऐल्कीनों से ऐल्केन तथा साइक्लोऐल्केन में परिवर्तित करने के लिए किया जाता है|
• इसका उपयोग वनस्पति तेलों से वनस्पति घी तैयार करने के लिए भी किया जाता है|
13. दिए गए हाइड्रोकार्बन: C2H6, C3H8, C3H6, C2H2 एवं CH4 में किसमें संकलन अभिक्रिया होती है?
उत्तर
असंतृप्त हाइड्रोकार्बनों में संकलन अभिक्रिया होती है| असंतृप्त हाइड्रोकार्बन होने के कारण C3H6 तथा C2H2 में संकलन अभिक्रिया होती है|
14. मक्खन एवं खाना बनाने वाले तेल के बीच रासायनिक अंतर समझने के लिए एक परीक्षण बताइए|
उत्तर
मक्खन में संतृप्त वसा होता है| अतः यह हाइड्रोजनीकृत नहीं हो सकता है| वहीँ दूसरी ओर, खाना पकाने वाले तेल में असंतृप्त वसा होता है, इसलिए यह संतृप्त वसा में हाइड्रोजनीकृत हो सकता है|
15. साबुन की सफाई प्रक्रिया की क्रियाविधि समझाइए|
उत्तर
साबुन के अणु ऐसे होते हैं जिनके दोनों सिरों के विभिन्न गुणधर्म होते हैं| जब साबुन जल की सतह पर होता है तब इसके अणु अपने को इस प्रकार व्यवस्थित कर लेते हैं कि इसका आयनिक सिरा जल के अंदर होता है जबकि दूसरा सिरा हाइड्रोकार्बन पूँछ जल के बाहर होता है| जल के अंदर इन अणुओं की एक विशेष व्यवस्था होती है जिससे इसका हाइड्रोकार्बन सिरा जल के बाहर बना होता है| ऐसा अणुओं का बड़ा गुच्छा बनने के कारण होता है जिसमें जलविरागी पूँछ गुच्छे के आंतरिक हिस्से में होती है जबकि उसका आयनिक सिरा गुच्छे की सतह पर होता है| इस संरचना को मिसेल कहते हैं| मिसेल के रूप में साबुन स्वच्छ करने में सक्षम होता है क्योंकि तैलीय मैल मिसेल के केंद्र में एकत्र हो जाते हैं| इस प्रकार साबुन का मिसेल मैल को पानी में घोलने में मदद करता है तथा कपड़े साफ़ हो जाते हैं|
प्रोपेनोन


